 百科 检测留言
百科 检测留言洁净室(区)环境检测流程是什么?洁净室(区)环境检测哪些项目?执行标准有哪些?检测报告有效期多久?做检测,找百检。百检第三方检测主要为公司企业、个体商户、高校科研提供检测服务。我们只做真实检测。
检测报告图片

风速、噪声、悬浮粒子/尘埃数、手表面细菌菌落总数、换气次数/风量、气流的检测、沉降菌、浮游菌、温度、照度、物体表面细菌菌落总数、相对湿度、自净时间、静压差、高效过滤器检漏、尘埃(悬浮)粒子、换气次数、悬浮粒子、风速及换气次数、压差、工人手表面细菌总数、工作台表面细菌菌落总数、气流流型、洁净度、湿度、空气中细菌菌落总数、风量、沉降菌测试、下降气流流速、主实验室排风高效过滤器检漏、垂直气流平均速度、室内送风量、回风量(排风量)、工作区的截面*低风速、工作窗口气流平均速度、工作窗口气流流向、振动、*小新风量、气流模式、气流流向、洁净度级别
检测标准:1、YY0569-2011 Ⅱ级生物安全柜
2、药品生产质量管理规范(2010年修订) 第三章
3、2007年版 化妆品生产企业卫生规范
4、GB/T 16294-2010 医药工业洁净室(区)沉降菌测试方法
5、GB T16294-2010 医药工业洁净室(区)沉降菌的测试方法
6、2001年 医疗机构制剂配制质量管理规范
7、GB/T16293-2010 医药工业区洁净室(区)浮游菌的测试方法
8、2015年 医疗器械生产质量管理规范
9、GB50333-2013 医院洁净手术部建筑技术规范 <13.3.6>、<13.3.7>
10、GB50591-2010 洁净室施工及验收规范
11、2010 药品生产质量管理规范
12、2020年版 中国药典 四部通则9205
13、YBB 00412004-2015 药品包装材料生产厂房洁净-室(区)的测试方法
14、DB31/T687-2013 临床细胞治疗技术平台设置基本要求
15、GB 50591-2010 洁净室施工及验收规范
16、YY 0569-2011 Ⅱ级生物安全柜 5.4.9
17、GB 50333-2013 医院洁净手术部建筑技术规范
18、2009 消毒产品生产企业卫生规范
19、YBB00412004-2015 药品包装材料生产厂房洁净室(区)的测试方法 <6>
20、2007 化妆品生产企业卫生规范
报告资质:
CMA;CNAS, 中文报告、英文报告、中英文报告。
检测报告作用:
电商平台入驻;商超卖场入驻;产品质量改进;产品认证;出口通关检验等
检测费用:
因检测项目及样品数量、实验复杂程度不同,具体费用请联系我们确定项目后方可报价。
检测报告有效期:
常规来说只要测试没更新,测试不变检测报告一直有效。一般检测报告上会标注实验室收到样品的时间、出具报告的时间。如果是用于过电商平台,一般他们只认可一年内的。所以还要看平台或买家的要求。
检测流程
以上内容为部分列举,仅供参考。百检也可根据您的需求设计检测方案。如果您对洁净室(区)环境检测有严格要求,不妨考虑选择我们的检测服务。更多信息请咨询客服。


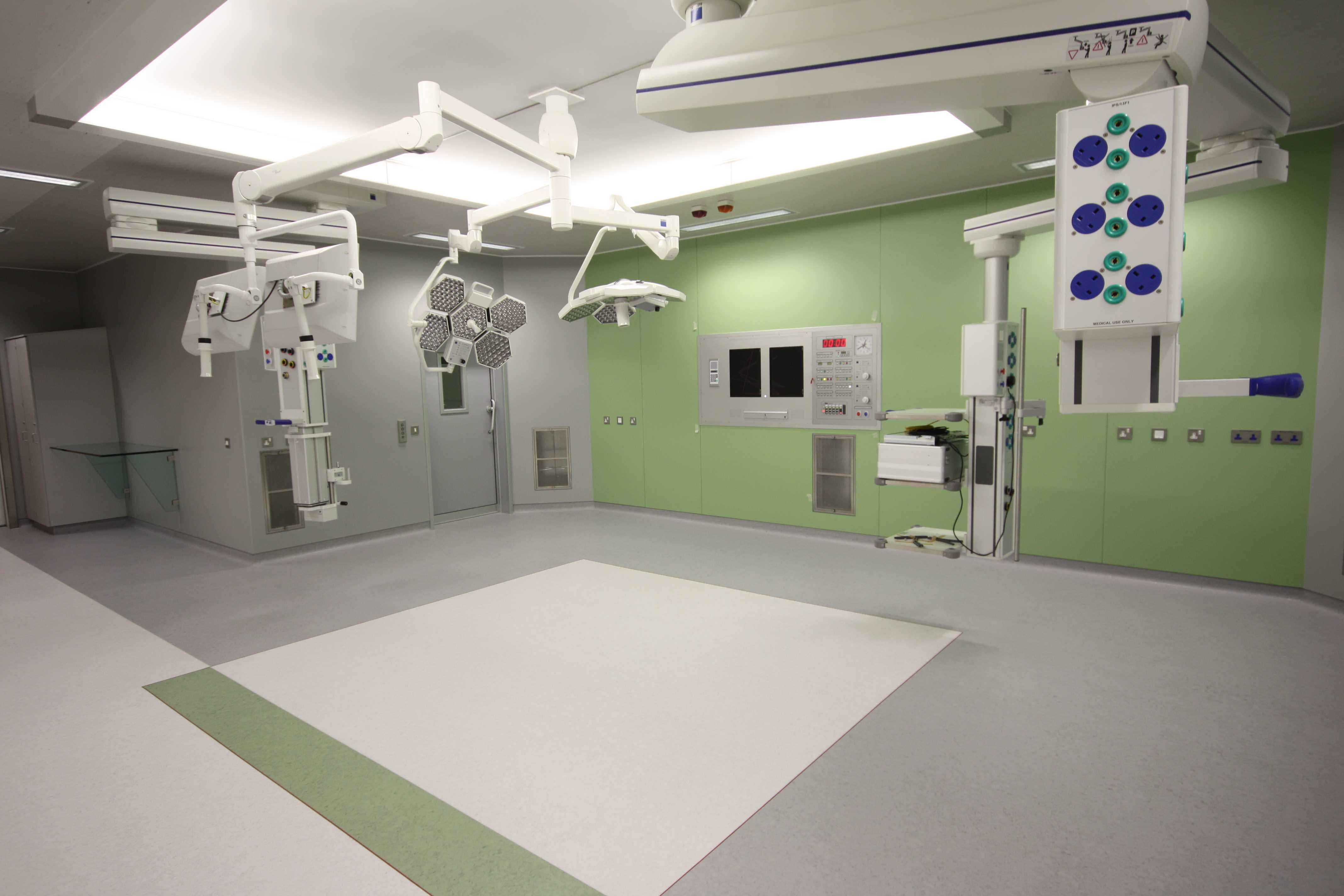
 1st洁净室环境检测实验室
1st洁净室环境检测实验室





















 400-101-7153
400-101-7153 15201733840
15201733840

