 百科 检测留言
百科 检测留言医药工业洁净室(区)检测报告如何办理?测试哪些项目?测试标准有哪些?百检也可依据相应检测标准或者根据您的需求设计检测方案。我们只做真实检测。
检测报告图片

沉降菌、悬浮粒子计数、微粒计数浓度、洁净度、工人手表面细菌菌落总数、工作台表面细菌菌落总数、悬浮粒子、换气次数、浮游菌、温度、相对湿度、静压差、悬浮粒子数、微粒计数浓度(悬浮粒子)、温度湿度、风速、悬浮粒子浓度、湿度、气流方向、照度、表面电阻、送风管风量、风量、沉降菌菌落数、浮游菌浓度、悬浮粒子测试、压缩气体粒子测定、压缩气体菌落数测定、手表面、工作台面细菌菌落总数、全部项目、全部参数、噪声、悬浮微生物、自净时间、高效过滤器检漏、沉降菌数、浮游菌数、风量与换气次数、浮游菌测试、沉降菌测试、表面微生物
检测标准:1、GB 50457-2019 医药工业洁净厂房设计规范 GB 50457-2019
2、GB/T 16294-2010 医药工业洁净室(区)沉降菌测定方法/
3、GB/T50591-2010附录E 温度
4、GB 50243-2016 《通风与空调工程施工质量验收规范》 GB 50243-2016
5、GB/T 16292-2010 医药工业洁净室(区)悬浮粒子的测试方法 GB/T 16292-2010
6、GB/T16293-2010 医药工业洁净室(区)浮游菌的测试方法
7、YY/T 0033-2000 《无菌医疗器具生产管理规范》 YY/T 0033-2000
8、ISO 14644.1-2015 洁净室及相关受控环境第1部分:空气洁净度等级 附录 A
9、GB 50457-2008 医药工业洁净厂房设计规范 3.2.1
10、GB 50073-2013 《洁净厂房设计规范》 附录A3.5
11、中国药典 2020版 四部 药品洁净实验室微生物监测和控制指导原则 9205
12、国家药监局令 第27号 医疗机构制剂配置质量管理规范 表Ⅱ
13、GB 50591-2010 洁净室施工及验收规范 附录E.4
14、GB 15979-2002 一次性使用卫生用品卫生标准 GB 15979-2002
15、YY 0569-2011 II级生物安全柜 6.3.7、6.3.8
16、GB/T 25915.3-2010 洁净室及相关受控环境 第3部分:检测方法 B4
17、GB 50073-2013 《洁净厂房设计规范》 GB 50073-2013
18、YY/T 0033-2000 《无菌医疗器具生产管理规范》 (附录C)
19、GB/T 16292-2010 医药工业洁净室(区)悬浮粒子的测试方法 5.4
20、GB15979-2002 一次性使用卫生用品卫生标准 附录 E2
检测报告用途商超入驻、电商上架、内部品控、招投标、高校科研等。
检测报告有效期一般检测报告上会标注实验室收到样品的时间、出具报告的时间。检测报告上不会标注有效期。常规来说只要测试没更新,测试不变检测报告一直有效。如果是用于过电商平台,一般他们只认可一年内的。所以还要看平台或买家的要求。
检测费用价格因测试项目及实验复杂程度不同,具体请联系客服确定后进行报价。
检测流程


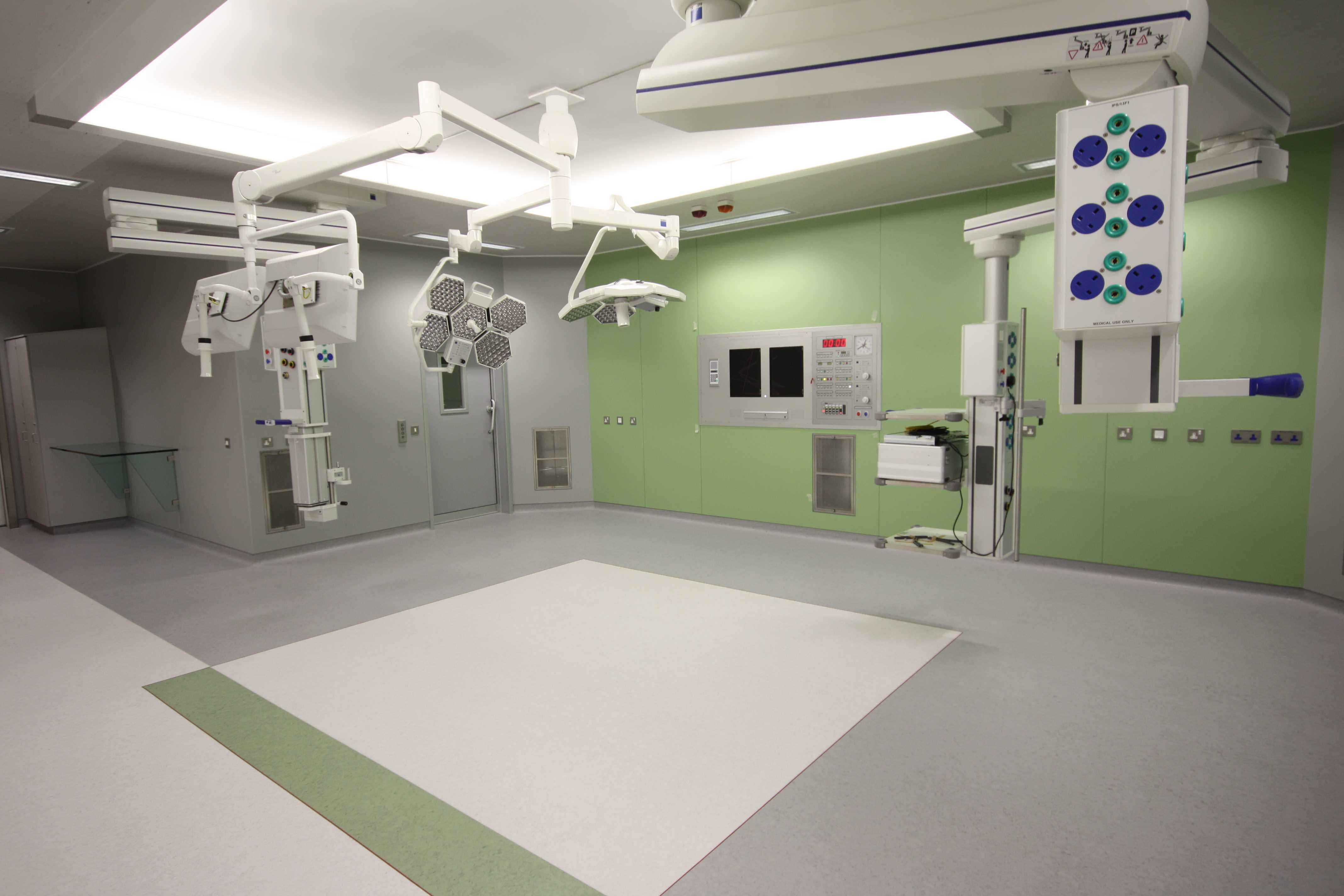
 1st医药工业洁净室(区)检测认证测试报告
1st医药工业洁净室(区)检测认证测试报告





















 400-101-7153
400-101-7153 15201733840
15201733840

